衰老影响CD4+ T细胞:效应/记忆平衡
理论上,在人体细胞衰老(aging)的过程中,T细胞活性失调受到外源性炎症性衰老的影响,幼稚T细胞数量降低,TCR的多样性和信号转导能力都会逐渐减弱。
但实际上,健康老年人体内的幼稚CD4+ T细胞数量依然庞大,且富有多样性。目前认为,这是适应性免疫中信号传导缺陷和过度驱动效应细胞分化的一种表现。
衰老CD4+ T细胞:如何启动短期效应程序
在年轻人的细胞中,TCR信号弱通常代表着记忆T细胞(Tm)形成增加。但在老年人细胞中,TCR信号弱反而使T细胞更多的向效应T细胞(Teff)分化。
Teff细胞的寿命远短于Tm。随着年龄增长,Teff亚群出现的频率越高,有助于增加炎症介质的产生。
这一表现并非是年龄依赖性的。动力学检测显示,无论是年轻人还是老年人,在不同强度TCR信号刺激下,二者的表观遗传变化动力学变化没有显著差异。
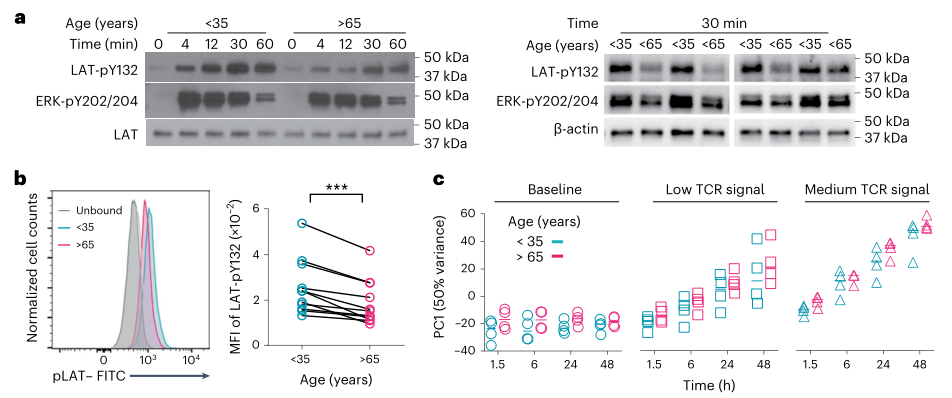
Nat Immunol 24, 96–109 (2023).
在健康年轻人中:
CD4+ T细胞分化的聚集亚群与选择性TF的富集相关,FR1、NF-κB和NUR77对其有调控作用。青年人特有的聚类在进一步分化之前的早期阶段显示出快速变化,随后进入24小时的平稳期。该簇上富集T细胞活化通路。
健康老年人CD4+ T细胞聚类则没有显示任何TF基序显著富集。

Nat Immunol 24, 96–109 (2023).
转录因子HELIOS则是IL-2RA的上游调控因子,可能直接抑制年轻人T细胞中IL2RA的表达。
在健康老年人中:
研究人员认为,衰老CD4+ T细胞受TCR信号刺激的这种异质性适应性免疫缺陷的原因可能是由表观遗传引发。
TCR刺激后,年轻人和老年人幼稚CD4+ T细胞表观遗传和转录变化的轨迹显示:尽管信号分子磷酸化减少,幼稚CD4+ T细胞的染色质可及性反应在老年人中反而更高。
STAT5是这种变化的主要驱动TF。STAT5的活性在TCR信号刺激的早期就升高并趋于平稳,IRF4活性则在24小时达到平稳,而BATF活性在48小时仍在上升。
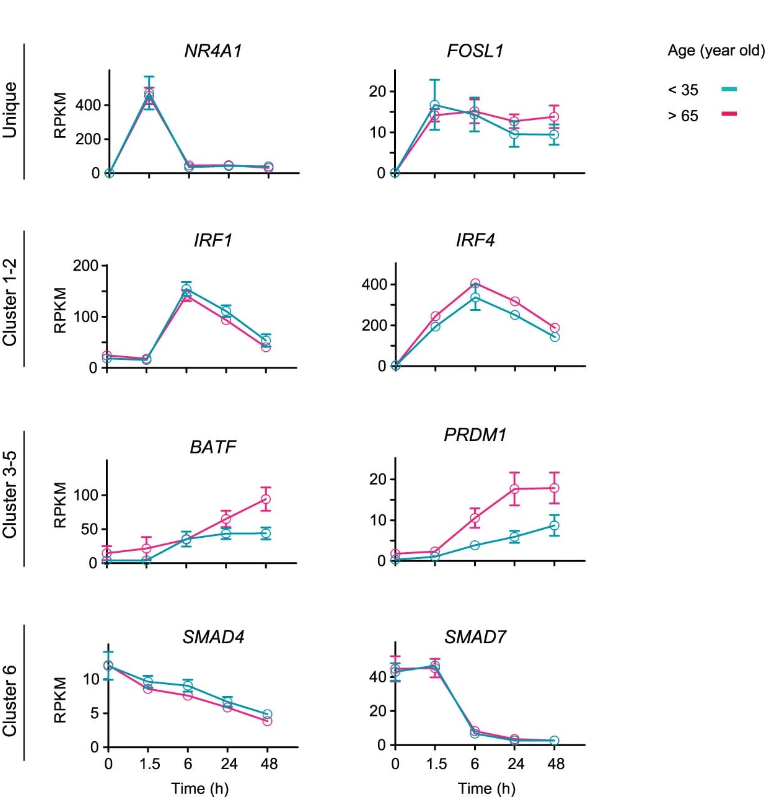
Nat Immunol 24, 96–109 (2023).
- 随着年龄增加,STAT5活性也增加,幼稚CD4+ T细胞亚群也随之扩增。
- 这种早期的STAT5活性是由幼稚T细胞上的CD25早期上调所引起的。
- CD25上调则是由转录因子HELIOS随年龄增长而丧失所引起的。
- BACH2在老年人中的低表达则可能使老年人的T细胞更容易被激活。
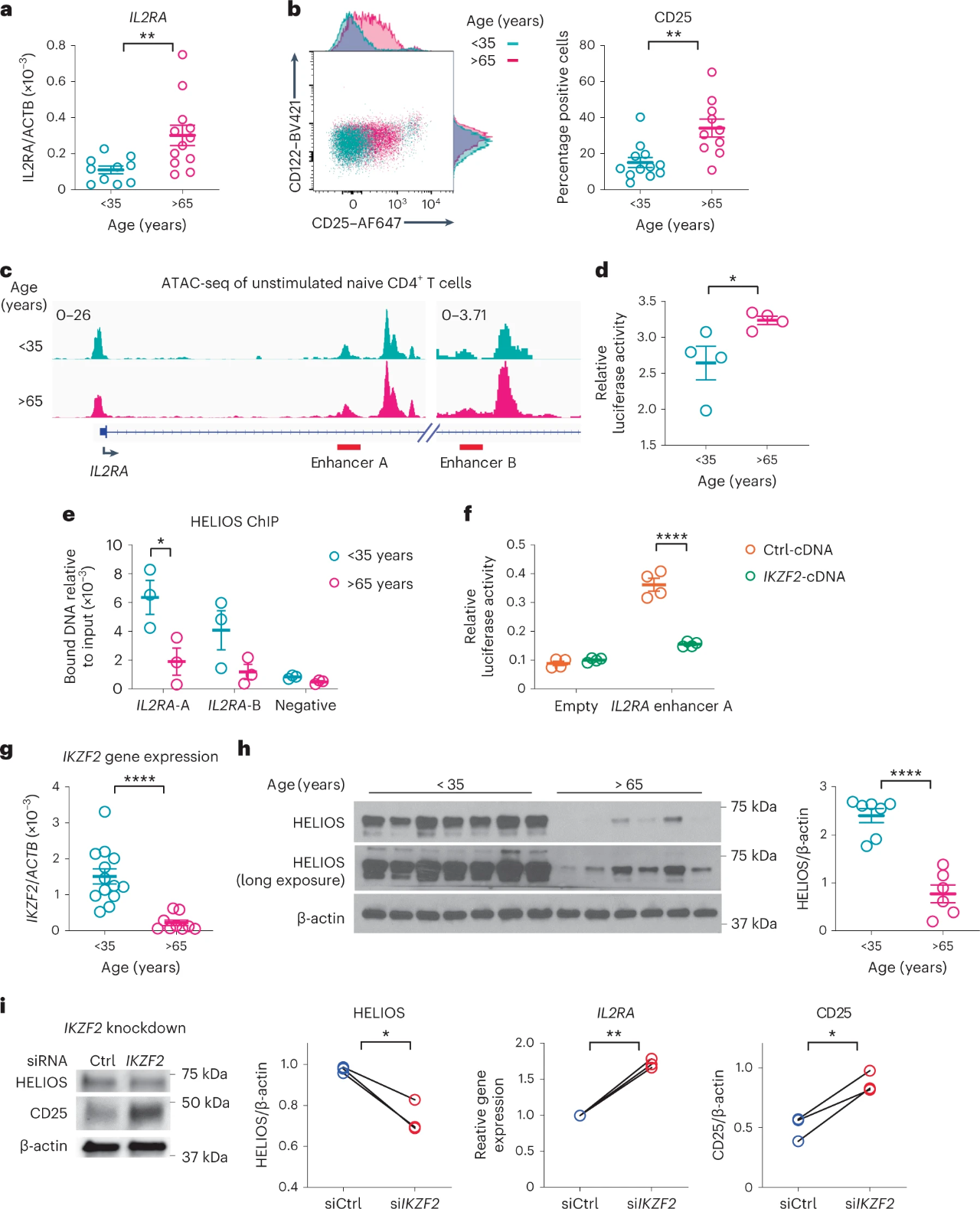
Nat Immunol 24, 96–109 (2023).
抑制STAT5信号通路可以重新确定老年人中幼稚CD4+ T细胞的表观遗传情况,并通过减少BLIMP1表达和增加TCF1来抑制促炎效应细胞的形成。
IL-2Rα则是STAT5信号的上游调控因子。来自老年人的CD4+ T细胞增加了对IL2RA转录物和IL-2Rα蛋白的表达,增加了磷酸化STAT5的丰度,增加了STAT5调控的转录因子的表达。
若抑制IL-2Rα信号或STAT5激活信号,使HELIOS、IL-2Rα和STAT5之间达到一定平衡,则能够在很大程度上消除衰老CD4+ T细胞启动短期效应程序的倾向,使其至少能恢复一些年轻细胞的典型特征。
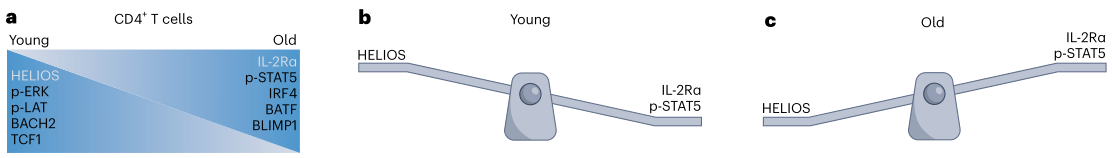
Nat Immunol 24, 8–9 (2023).
小结
总体而言:TCR信号的失调和IL-2通路有关,通过表观遗传重编程影响衰老CD4+ T细胞分化倾向。
- 衰老影响HELIOS和IL2RA表达之间的平衡;
- IL-2Rα和STAT5的活性反过来调节CD4+ T细胞的下游表观遗传重编程潜能。
CD4+ T细胞分化是维持长期免疫反应的重要来源。在健康人中,IL-2Rα信号通路随着年龄的增长而增强,而TCR信号通路则减弱。二者本是同时对CD4+ T细胞进行复杂影响,并还影响着其他免疫细胞亚群。因此是否能够通过三者平衡简单地达到恢复免疫活性的目的,还有待商榷。
参考文献:1.Weinmann, A.S. Tipping the balance in CD4+ T cells. Nat Immunol 24, 8–9 (2023). https://doi.org/10.1038/s41590-022-01389-72.Zhang, H., Jadhav, R.R., Cao, W. et al. Aging-associated HELIOS deficiency in naive CD4 T cells alters chromatin remodeling and promotes effector cell responses. Nat Immunol 24, 96–109 (2023). https://doi.org/10.1038/s41590-022-01369-x+来源:老闲谈 Immunology 2023-01-11